企業治験・医師主導治験等をご検討されているお客様へ
 化合物安全性研究所では、非臨床試験及び臨床試験(企業治験及び医師主導治験等のモニタリング・監査業務・PK測定業務等)を受託しております。ご予算に応じ、受託業務の範囲等フレキシブルに対応することが可能です。
化合物安全性研究所では、非臨床試験及び臨床試験(企業治験及び医師主導治験等のモニタリング・監査業務・PK測定業務等)を受託しております。ご予算に応じ、受託業務の範囲等フレキシブルに対応することが可能です。
臨床試験における受託可能な業務に関しましては臨床試験関連のページをご参照ください、非臨床から臨床へのスムーズな橋渡しをサポートいたします。
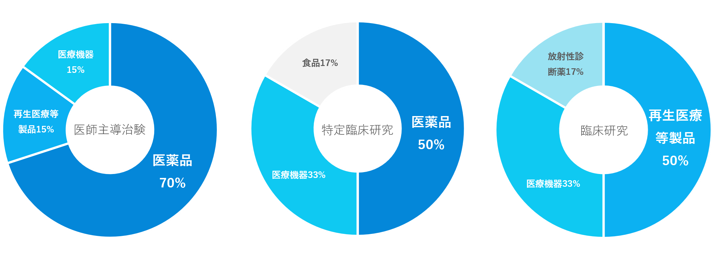
受託実績
医薬品・医療機器・再生医療等製品における非臨床安全試験に加え、臨床試験におけるCRO業務のご依頼が増加しています。
大学病院からの分類別受託実績
受託業務
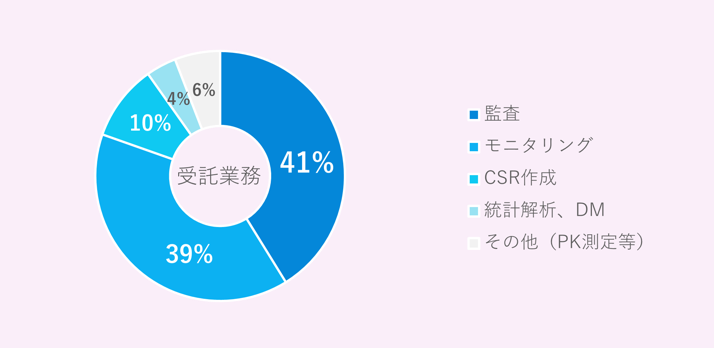
化合物安全性研究所が受託している臨床試験業務は以下の通りです。
- 治験調整医師の標準業務手順書(SOP)の作成支援
- 調整事務局業務
- モニタリング業務
- メディカルライティング業務
- 症例登録・症例報告書システム開発・保守業務
各種手順書作成
体制構築支援、キックオフミーティング開催支援
治験届提出支援
治験実施計画書・同意説明文書等必須文書作成支援、管理、資料保管
実施医療機関手続き・IRB対応支援、問い合わせ対応
医療機関でのスタートアップミーティングの開催
治験製品提供者との調整業務
治験製品の中央管理業務
各委託業者との調整支援
QMPに基づく品質管理
医師主導治験保険加入に係る各種調整及び加入手続き
被験者組入れ促進、進捗状況確認
症例検討会開催支援
jRCT等情報公開サイトへの試験情報登録・管理・更新
手順書/計画書作成
モニタリング(必須文書閲覧、SDV)
各種会議、症例検討会参加
総括報告書(案)作成
症例登録・報告書システム(EDC)の構築及び関連文書の作成
EDCライセンス
システム運用・保守・修正
バージョンアップ
- データマネジメント業務
- 統計解析業務
- 監査業務
- 安全性情報管理
手順書/計画書作成
データマネジメント運用業務
データクリーニング業務
効果安全性評価委員会の資料作成
症例検討会資料の作成支援
データ固定業務
修了業務(電子署名依頼対応)
統計解析計画の作成
解析用データセット作成プログラムの作成
解析プログラムの作成
固定データを用いた解析結果の作成・検証
作業記録の整備・業務終了手続き
手順書/計画書作成
医療機関監査
総括報告書監査
監査報告書の作成
手順書作成
管理業務
安全性情報発生時の対応
当局報告書作成*
定期報告書案作成*
文献検索
* 治験製品販売元からの情報提供があった場合には対応が可能です。
※一部業務は他社への再委託となる場合がございます。
お問い合わせはこちら
~非臨床試験から臨床試験まで
ワンストップサポート~
試験のご依頼・ご相談はお気軽にお問い合わせください。